张觉超
《Cell》杂志发表
每一台徕卡设备都有它*的定位,我们要做的就是保证其经得起时间的考验,发挥它们应有的价值。今天,给大家带来的是徕卡客户用共聚焦产品SP5在《Cell》杂志上发表的题为“Inhibition of SARS-CoV-2 Infections in Engineered Human Tissues Using Clinical-Grade Soluble Human ACE2”的研究论文[1]。关注研究热点的同时给大家介绍一下徕卡显微镜对研究体系建立的助益。
进入2020年,科研人员们火力全开,为尽早开发出“解药”而争分夺秒。另一方面,主流期刊不吝篇幅地报导科研工作者们的研究进展。学术期刊《Cell》于4月24日刊发了一篇由三个科研团队(瑞典卡罗琳斯卡学院、西班牙巴塞罗那理工学院和奥地利科学院)的科学家们联合发表的研究论文,研究指出,hrsACE2(重组可溶性人源血管紧张素转化酶2)能有效抑制病毒对宿主细胞的感染(图1)。值得注意的是,该研究使用的hrsACE2蛋白作为一种治疗急性呼吸窘迫综合征(ARDS)的药物,已经通过了I期和II期的临床试验[2,3],后续临床转化指日可待。
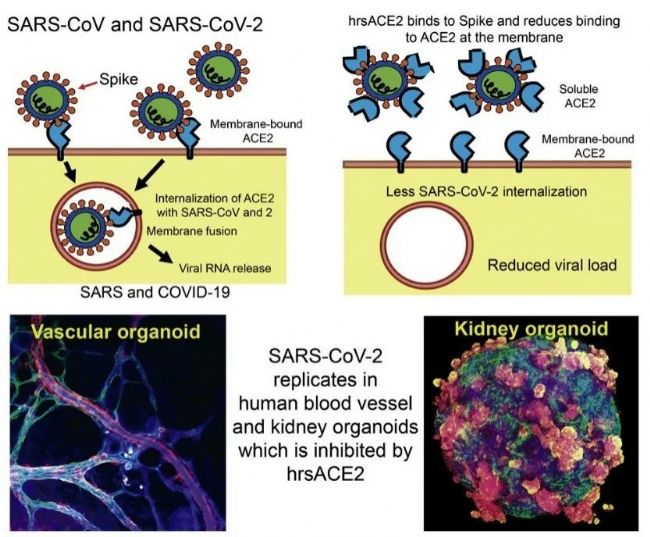
图1 论文图文摘要[1]
介绍研究结果之前,让我们先了解一下这篇论文使用的研究体系,作者是在一种工程化组织——类器官(Organoid)中开展的研究。类器官是由多能干细胞或特定器官来源的祖细胞在体外培养条件下分化形成的器官样组织[4]。目前,科研工作者已成功实现对肠道、肝脏、肾脏、大脑等许多组织的类器官培养,并将其运用到疾病模型建立、药物筛选、药物安全性评价等相关研究中(图2)。可以说,类器官算是在学术界“小有名气”的研究体系了,其相关研究的文章不乏大牛之作。2017年,类器官体系还被《Nature Method》杂志评选为2017年度技术[5]。我们今天关注的研究中就利用了人源血管类器官和肾脏类器官(图1)。
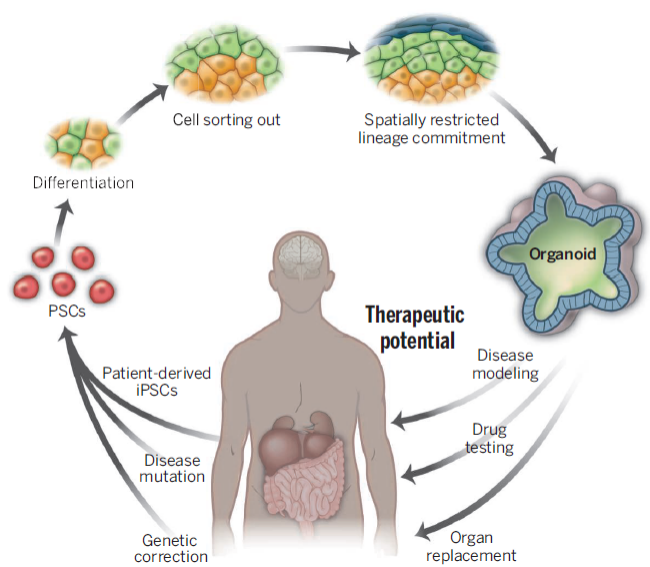
图2 类器官制备和应用前景简图[4]
知识点:类器官的*特性[4]
(1) 必须包含原器官特异性的细胞;
(2) 必须表现出原器官一些*的功能;
(3) 必须形成与原器官相似的结构。
言归正传,我们看看今天这篇《Cell》论文是如何“养成”的。由于病毒与2003年SARS病毒存在一定的相似性,科学家们很快找到病毒在宿主细胞表面的关键受体ACE2(与SARS病毒受体相同)。作为“ACE2是SARS病毒刺突蛋白(Spike protein)受体”的发现团队,本文的作者们长期关注ACE2蛋白的功能以及相关药物的研究动向,想到了用临床级hrsACE2阻断病毒表面刺突与宿主ACE2蛋白结合从而抑制其感染能力(图1)。研究思路清晰后,实验在团队协作下快速推进,在分离和鉴定病毒后,作者先通过实验确定hrsACE2能特异性的抑制病毒对细胞株的感染(图3)。
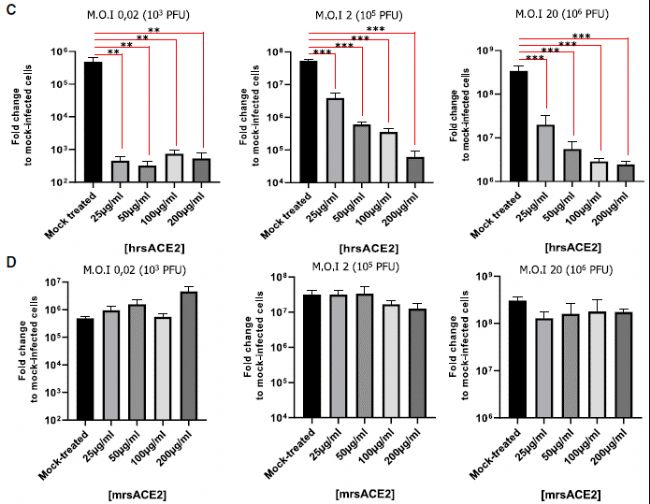
图3 hrsACE2抑制病毒的细胞感染能力[1]
在鼠源重组可溶性ACE2(mrsACE2)处理组为阴性结果的衬托下,细胞实验完美收官,结果喜人。为了进一步验证hrsACE2在组织内的作用,作者选用了类器官研究体系检测了hrsACE2蛋白对病毒二次感染能力的影响。血管类器官(图4)和肾脏类器官(图5)中的结果显示hrsACE2能有效抑制病毒对类器官的感染。其中,精美清晰的类器官标志分子共聚焦检测图片和红线高亮的统计学差异也足以打动《Cell》的主编和审稿人。
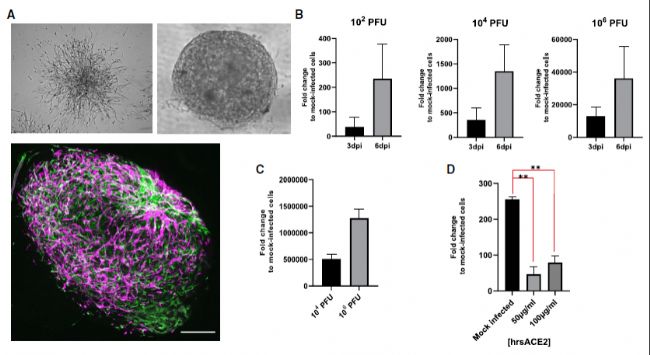
图4 hrsACE2抑制病毒感染血管类器官[1]
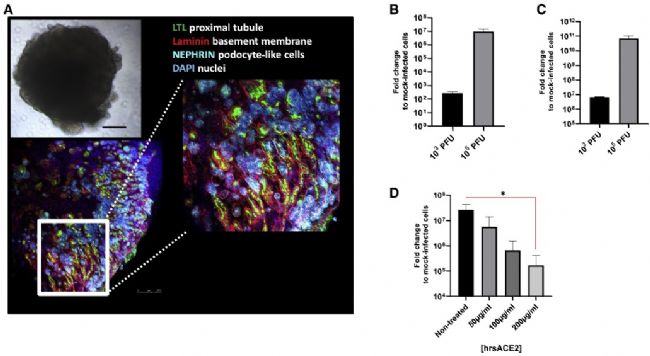
图5 hrsACE2抑制病毒感染肾脏类器官[1]
恭喜客户的研究论文行云流水般刊稿。不得不提,这篇文章从2月分离得到毒株到4月文章《Cell》见刊,笔者对研究组的工作效率真是佩服到“orz”。
感叹该研究团队飞一般工作效率之余,让我们关注一下作者使用的共聚焦产品——徕卡SP5,真可谓老骥伏枥,志在千里!SP5的上市时间可以追溯到2005年,时至今日,我们正在经历SP8(2012年上市)的时代,即将迎来徕卡共聚焦新品STELLARIS的时代(敬请密切关注徕卡近期产品发布信息)。然而,每一年在高水平期刊发表的大作中,仍能看到SP5共聚焦“助攻”研究的佳作。足以看出徕卡产品的稳定性受到研究体系的青睐。
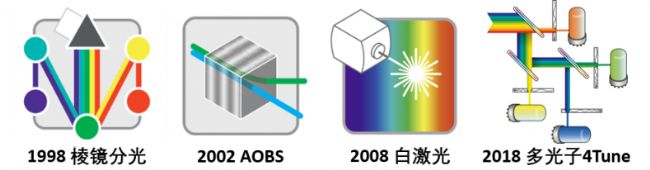
图6 徕卡共聚焦光谱成像研发历史
徕卡在共聚焦领域的研发生产,历史悠久,各种创新设计不胜枚举(图6)。早在1998年,徕卡革命性地使用了棱镜分光来替代滤片分光,带领共聚焦成像跨入了光谱时代;2002将万能的声光可调分光器AOBS引入共聚焦,取代传统的二向色镜;2008年又再次开创性地将白激光引入共聚焦领域。白激光、AOBS及棱镜分光三者的完美结合,使得共聚焦成像在光谱维度上同时实现了激发、分光以及发射三方面的*自由。2018推出的DIVE多光子系统,通过创新的4Tune设计,*实现多光子NDD外置检测器的光谱自由,再一次带领多光子成像进入了光谱时代。
徕卡创新的脚步从未停止,那么徕卡共聚焦人下一个攻克的 “成像自由”会是哪个维度?徕卡又会带领共聚焦成像进入一个什么时代呢?敬请期待!
神秘共聚焦新品:STELLARIS

图7 徕卡共聚焦新品STELLARIS
参考资料:
[1] Vanessa M, Hyesoo K, Patricia P, et al. Inhibition of SARS-CoV-2 infections in engineered human tissues using clinical-grade soluble human ACE2. Cell, 2020, 181: 1–9
[2] Haschke M, Schuster M, Marko P, et al. Pharmacokinetics and Pharmacodynamics of Recombinant Human Angiotensin-Converting Enzyme 2 in Healthy Human Subjects. Clinical Pharmacokinetics, 2013, 52(9):783-792.
[3] Khan A, Benthin C, Zeno B, et al. A pilot clinical trial of recombinant human angiotensin-converting enzyme 2 in acute respiratory distress syndrome. Critical Care, 2017, 21(1):234.
[4] Lancaster MA, Knoblich JA. Organogenesis in a dish: Modeling development and disease using organoid technologies. Science, 2014, 345(6194):283-283.
[5] Method of the Year 2017: Organoids. Nature Methods, 2018, 15(1):1-1.
电话
微信扫一扫
