Cell dive助力《Science》发表,参见2025年 KLF2 maintains lineage fidelity and suppresses CD8 T cell exhaustion during acute LCMV infection 一文。
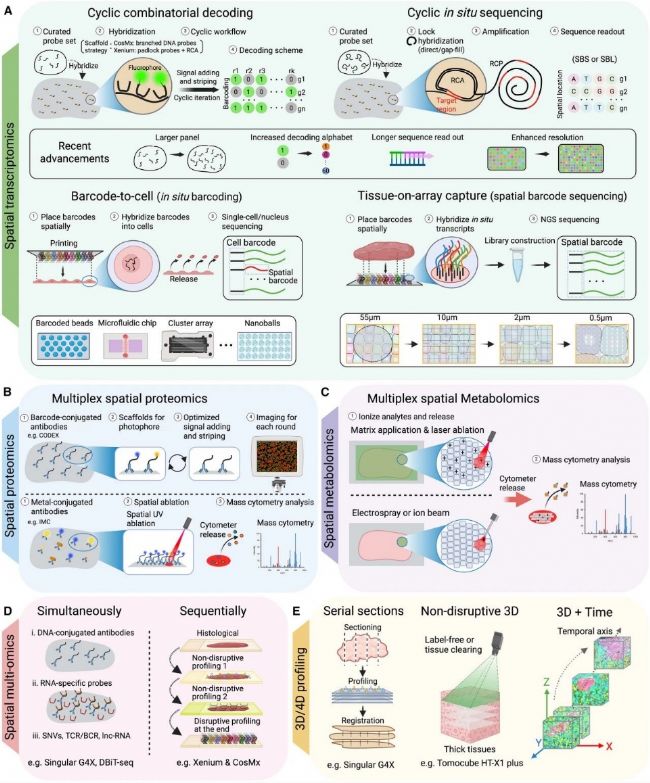
“2025年12月31日,国际期刊《Cancer Cell》发表德克萨斯大学MD安德森癌症中心王凌华教授团队的一篇空间组学重要综述。文章指出空间组学技术已步入成熟期,它通过揭示肿瘤细胞与微环境在组织原位的空间组织、相互作用和演化规律,以准确的精度重塑我们对癌症的认知。空间组学技术不仅是*的科研工具,更逐步成为下一代精准肿瘤学的临床基石。"
2025年2月14日,美国耶鲁大学Nikhil S. Joshi课题组Eric Fagerberg , John Attanasio , Christine Dien 等学者在《Science》 发布- KLF2 maintains lineage fidelity and suppresses CD8 T cell exhaustion during acute LCMV infection,关于LCMV急性感染期间KLF2维持谱系保真度并抑制CD8 T细胞耗竭的研究。
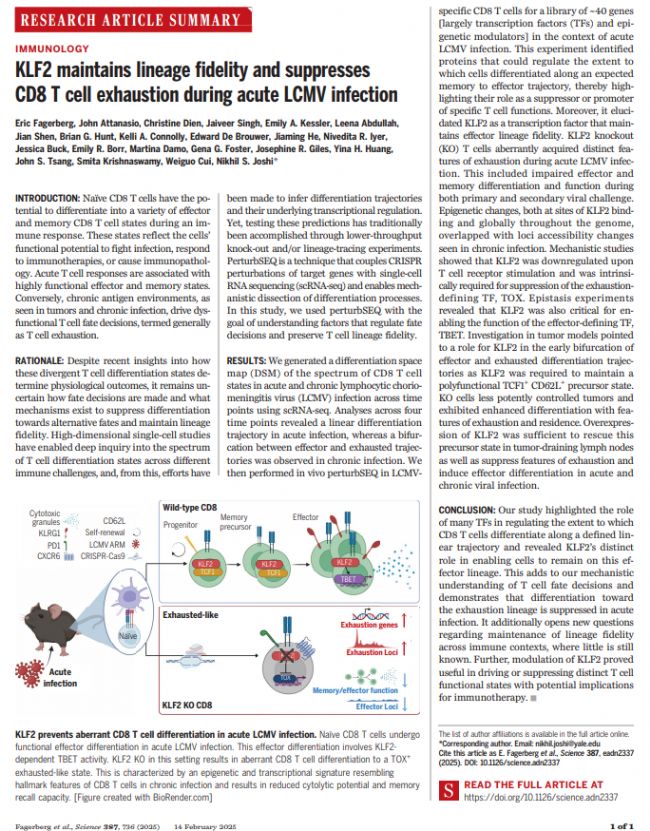
在免疫应答过程中,天然CD8 T细胞有潜力分化成功能状态广泛的细胞谱系。本研究采用基于CRISPR-Cas9 in vivo 核酸干扰评估T细胞命运决定中的约40种转录因子(TFs)和表观遗传调节模块,意外发现敲除TF Klf2导致急性感染期间异常分化成耗竭样CD8 T细胞。KLF2用来抑制促进耗竭的TF TOX,同时也是维持多功能肿瘤特异性祖细胞状态的关键。该结果表明KLF2提供效应CD8 T细胞谱系保真度,抑制耗竭程序。刷新认知:传统认为T细胞衰竭仅发生在慢性抗原环境中,本研究证明急性感染中也存在衰竭程序,但被KLF2主动抑制。
该研究构建了全面的分化空间图谱(DSM),整合急性和慢性LCMV感染多个时间点(第4、8、28、40天)的单细胞数据,揭示急性感染呈线性分化轨迹,慢性感染呈分叉轨迹(效应vs衰竭),为理解T细胞命运决定提供了研究框架。转化医学意义,KLF2过表达可抑制衰竭特征并促进效应分化,为肿瘤免疫治疗提供新的干预靶点。
该研究中显微成像设备为
Cell DIVE 超多标组织成像分析系统
01产品特点
多重免疫荧光成像:可同时检测超多标记物(可在一张切片对多达60个以上的markers成像)。
自发荧光控制:采用染料失活技术消除背景。
高分辨率:可观察组织内细胞空间分布,结合Aivia空间分析功能,完成空间生物学超多标批量处理,快速获得研究洞察。
02该研究中的价值
验证异常分化的
空间生物学免疫微环境
发现KLF2缺失的T细胞在第8天更多定位在髓区,提示其分化状态与正常效应T细胞的组织分布模式不同。
排除位置依赖性假说
分析数据支持KLF2的作用是位置独立的,主要通过内在转录调控而非微环境位置决定细胞命运。
03与其他技术的互补性
显微成像提供关键的空间信息,流式细胞术提供定量表型数据,单细胞测序提供转录组信息,ATAC-seq提供表观遗传信息,四者结合形成完整的研究体系。
丰富的研究方法将进一步深化细胞命运决定的理解,并可能带来新的免疫治疗策略。空间生物学,临床应用未来!
相关产品:
 编辑搜图
编辑搜图
CELL DIVE 超多标组织成像分析系统
电话
微信扫一扫
